Sonderforschungsbereich
Transregio 221
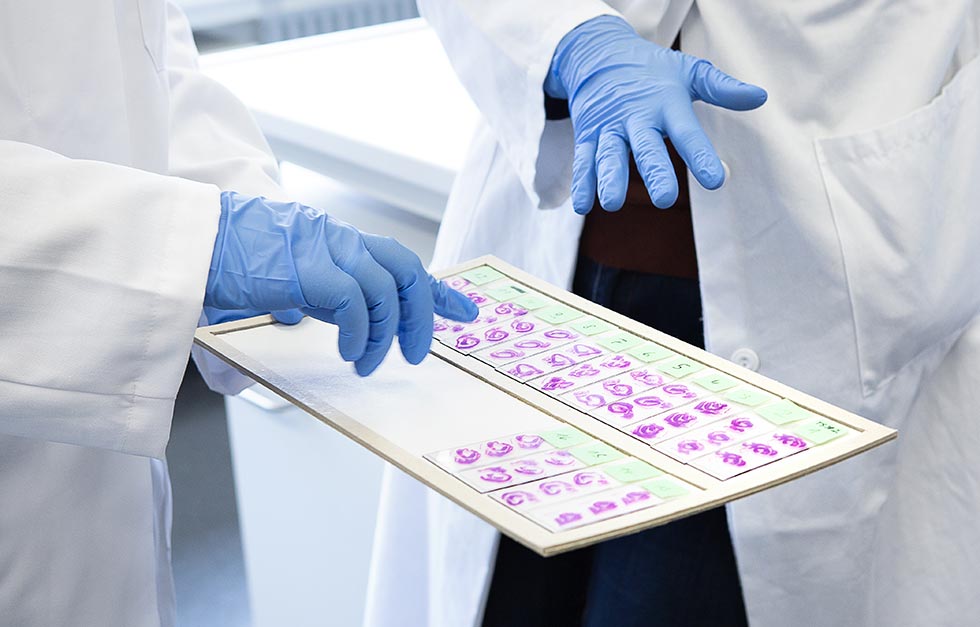
Wissenschaftler aus Regensburg, Erlangen und Würzburg arbeiten im neuen SFB zusammen. Im Fokus stehen dabei bislang ungelöste Herausforderungen bei der Therapie von Leukämie- und Lymphompatienten.
Sonderforschungsbereich
Transregio 221
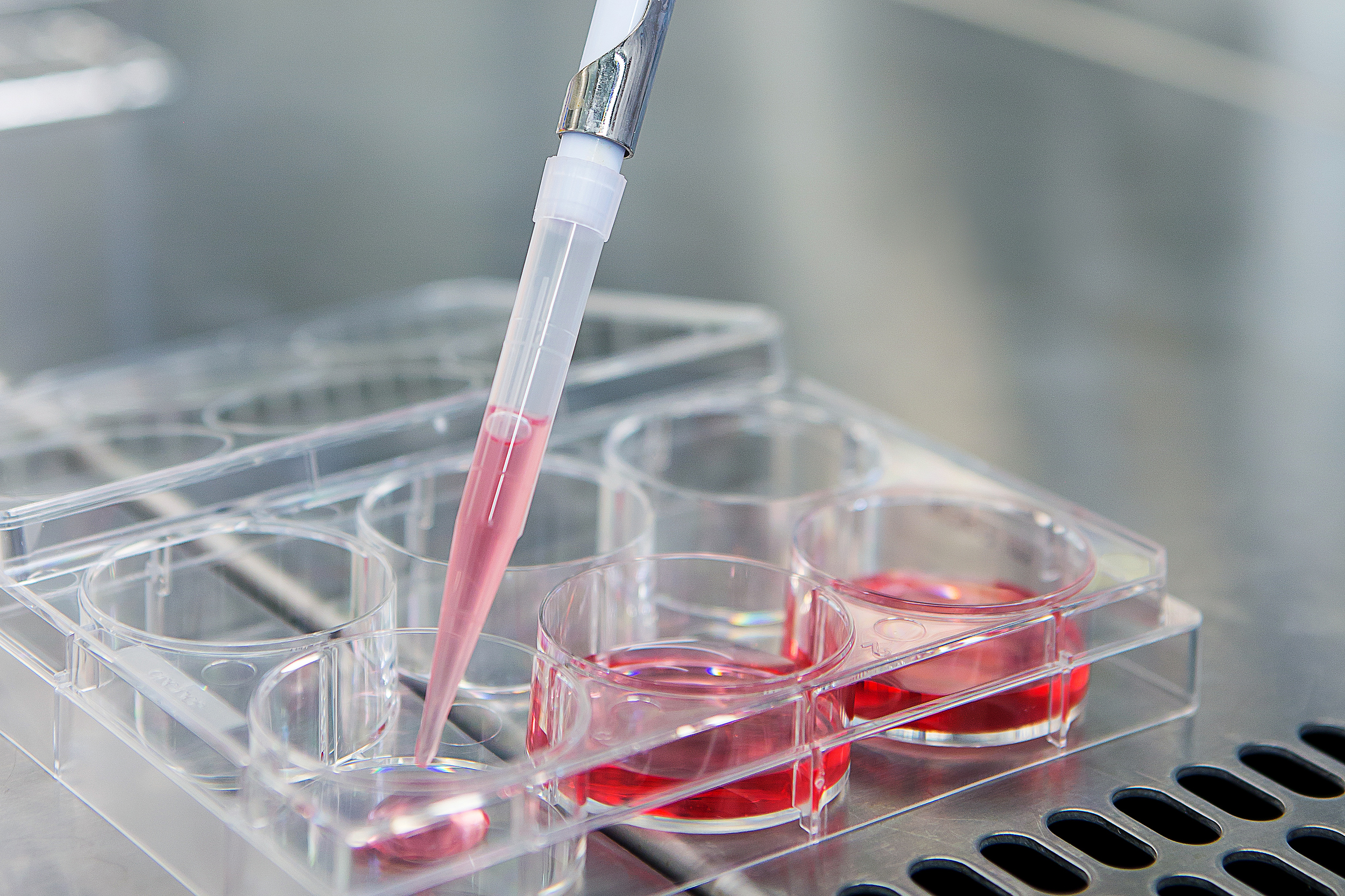
Ziel der Wissenschaftler ist die Verbesserung der allogenen hämatopoetischen Stammzelltransplantation durch Modulation der Transplantat-gegen-Wirt- und Trans- plantat-gegen-Leukämie-Immunreaktionen.

Immer mittwochs
KMT-Lunchseminar
13:00 bis 14:00 Uhr
Standort: Universitätsklinikum Regensburg
Beim Laden der Karte werden externe Inhalte und Cookies von Google Maps geladen.
Nähere Informationen entnehmen Sie unserer Datenschutzerklärung.
Beim Laden des Videos werden externe Inhalte und Cookies von YouTube geladen.
Nähere Informationen entnehmen Sie unserer Datenschutzerklärung.
Was ist|Transregio 221?
Im Sonderforschungsbereich Transregio 221 wollen Immunmediziner und Wissenschaftler der Universitäten Regensburg, Erlangen und Würzburg und der dortigen Universitätsklinika gemeinsam Wege finden, die allogene Stammzelltransplantation zukünftig sicherer und erfolgreicher zu machen, indem Krankheitsrückfälle vermieden und Transplantationskomplikationen vermindert werden.
Was ist eine|Stammzelltransplantation?
Die allogene hämatopoetische Stammzelltransplantation (HSZT) ist eine kurative Therapiemöglichkeit bei Chemotherapie-refraktären Leukämie- und Lymphomerkrankungen sowie bei angeborenen oder erworbenen Defekten der Blutbildung. Weltweit wurden bis heute etwa eine halbe Million Transplantationen durchgeführt und 28 Millionen freiwillige Stammzellspender registriert. Neben dem Austausch der erkrankten Hämatopoese durch die gesunden Stammzellen des Spenders beruht die therapeutische Wirkung der HSZT vor allem auf der immunologisch vermittelten Eliminierung von hämatopoetischen Patientenzellen durch kotransplantierte Spenderlymphozyten. Für diese sogenannte Transplantat-gegen-Hämatopoese-Reaktion sind hauptsächlich Spender T-Zellen verantwortlich, die sich auch gegen maligne hämatopoetische Zellen des Patienten richten, was als Transplantat-gegen-Leukämie-Effekt (graft-versus-leukemia, GvL) bzw. Transplantat-gegen-Lymphom-Effekt bezeichnet wird.
Was ist|GvL?
Der Transplantat-gegen-Leukämie- bzw. Transplantat-gegen-Lymphom-Effekt (graft-versus-leukemia, GvL) ist eine immunologische Reaktion der Spenderlymphozyten gegen im Patienten vorhandene Leukämiezellen. Dieser Effekt führt bei sehr vielen Patienten zu einer kompletten Eliminierung der Leukämie- und Lymphomzellen und damit zur Heilung des Patienten. Allerdings ist der GvL-Effekt bei etwa 20-30% der Patienten zu schwach, um sämtliche bösartige Zellen zu zerstören. Um dieses Wiederauftreten der Erkrankung (Rezidiv) zu verhindern, muss der GvL-Effekt besser verstanden werden und anschließend therapeutisch gezielt verstärkt werden, damit idealerweise sämtliche Patienten von ihrer Leukämie/bzw. Lymphom geheilt werden können.
Was ist|GvHD?
Weiterhin bleiben die immunologischen Wirkungen des Spenderimmunsystems nicht immer auf die Bekämpfung der Leukämie- oder Lymphomerkrankung beschränkt, sondern können sich auch gegen gesundes Körpergewebe des Patienten richten, was in der sogenannten Transplantat-gegen-Wirt-Erkrankung (graft-versus-host-disease, GvHD) resultiert. Die GvHD greift insbesondere die Haut, die Leber und den Darm an, bei der chronischen Variante sind aber auch zahlreiche andere Körpergewebe betroffen. An diesen zentralen Herausforderungen der Transplantationsmedizin setzt der Sonderforschungsbereich Transregio 221 an.
Was ist|das Ziel?
Im SFB untersuchen die beteiligten Wissenschaftler im Projektbereich A innovative Verfahren der T-Zell-Programmierung und -Reaktivierung (z. B. gentechnischer Transfer von T-Zell-Rezeptoren und chimären Antigen-Rezeptoren, Einsatz von multi-spezifischen Antikörpern, Immun-Checkpoint-Modulatoren und Minorhistokompatibilitätsantigen-spezifischen T-Zellen) für die gezielte Verstärkung des GvL-Effekts. Im Projektbereich B entwickeln die Wissenschaftler neue Strategien für die effektive Verhinderung oder Behandlung der GvHD durch die spezifische Modulation von Zellsignalwegen, regulatorischen Netzwerken der angeborenen und erworbenen Immunität sowie pathogenitätsrelevanter Kofaktoren (z. B. Gewebeentzündungsvorgänge und Mikrobiom-Veränderungen). Die Strategien zur Stärkung des GvL-Effekts werden jeweils hinsichtlich ihrer Auswirkungen auf die GvHD untersucht, während umgekehrt GvHD-supprimierende Interventionen bezüglich ihres Einflusses auf die GvL-Wirkung getestet werden. Erfolgversprechende Strategien dieser grundlagenwissenschaftlichen Arbeiten sollen mittelfristig in klinischen Studien überprüft werden, um die Sicherheit und Wirksamkeit der allogenen Stammzelltransplantation nachhaltig zu verbessern.